ЗОНА РИЗИКУ
Щороку понад 30 тисяч українців беруть участь у клінічних випробуваннях лікарських препаратів
Як відомо, фармацевтика — одна з найприбутковіших галузей. Світові інвестиції в розробку нових лікарських препаратів щорічно перевищують 100 млрд доларів. Утім, щоб нові ліки отримали реєстрацію і надійшли в продаж, вони повинні пройти клінічні випробування в максимальній кількості країн на різних континентах.
Довготривалий процес розробки інноваційного препарату включає кілька етапів. Після завершення програми доклінічних досліджень новий лікарський засіб проходить клінічне дослідження першої фази за участі людей (зазвичай невеликої кількості здорових добровольців), основною метою якої є оцінка його безпеки. Друга фаза виявляє фармакологічні властивості препарату, третя має засвідчити його безпеку й ефективність. Після успішного проходження всіх трьох фаз клінічних досліджень продукт реєструється як лікарський засіб.
— Загалом ми проти будь-яких досліджень на людині. Але є професійна позиція. Без клінічних досліджень не обійтися. Без пошуку кращих ліків з багатьма захворюваннями (онкологія, розсіяний склероз) боротися неможливо, — вважає заступник директора Державного експертного центру МОЗ України Анатолій Морозов.
Вартість клінічного дослідження одного препарату для фармкомпаній — сотні мільйонів доларів, але, виявляється, це варто того, адже протягом 10 або 15 років після його реєстрації компанія має монопольне право на його виробництво. Тільки після цього терміну інші компанії отримують право на випуск генериків (аналогів, зроблених іншими компаніями на основі діючої речовини цього препарату).
Приховати результати не вдасться
Існує думка, що країни третього світу використовуються західними фірмами як полігон для випробувань нових ліків (дехто вважає, що це стосується і України). Фахівці це заперечують.
— По-перше, в Україні випробування на здорових людях не проводяться вже понад 40 років. Як правило, препарати для клінічних досліджень надходять у нашу країну вже під час третьої фази — коли безпека активних інгредієнтів практично доведена, — зазначив голова Центральної комісії з питань етики МОЗ Василь Корнацький. — До речі, на відміну від України, більшість країн світу активно проводять першу фазу клінічних досліджень. 76% досліджень першої фази здійснюються в трьох країнах — США, Канаді та Нідерландах. По-друге, наявність таких досліджень позитивна для іміджу країни, адже це означає, що вона має сучасні клініки, які відповідають міжнародним нормам. Зрештою, фарм- компанія не зацікавлена в тому, щоб провести дослідження з порушенням правил, оскільки це зруйнує її імідж і негативно позначиться на долі нового препарату.
Підпільне проведення клінічних досліджень не має сенсу, адже препарат, що не пройшов офіційних клінічних досліджень, не може бути зареєстрований і виведений на фармацевтичний ринок. У дослідженнях беруть участь сотні фахівців і тисячі пацієнтів. Як можна приховати ці результати? Тож у країну, яка не має відповідної науково-технічної бази, фірми просто не підуть. Можу сказати, що Україна в цьому плані має досить позитивну репутацію. Понад 400 вітчизняних клінік отримали право на такі дослідження. А це означає надбавку до бюджету клінік, з якими працює зарубіжна фармкомпанія, освітні програми для лікарів, навчання новим технологіям, податки, які платять фірми до бюджету.
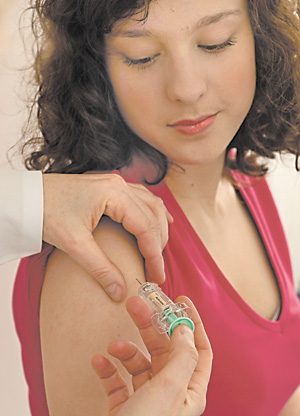
Перш ніж препарат надійде до споживача, його треба ретельно перевірити. Фото з сайту tk.de
Ліки безкоштовно
А що дають клінічні дослідження конкретно пацієнтам? Як стверджують фахівці, — шанс на одужання, адже у випробуваннях переважно беруть участь люди, які мають важкі захворювання. Найчастіше на них погоджуються онкологічні хворі, бо хочуть встигнути отримати краще лікування: а раптом винайшли щось нове? Тим більше, що ліки, навіть дорогі, такі пацієнти отримують безкоштовно (на відміну від всіх інших, яким доводиться платити за них з власної кишені). Компанія-спонсор або клініка зазвичай беруть на себе зобов’язання протягом усього процесу лікування «вести» своїх пацієнтів, безкоштовно забезпечувати ліками. За участь у дослідженнях пацієнтам не платять — це міжнародна практика.
— У нас для багатьох хворих це чи не єдиний шанс отримати безкоштовне лікування, — вважає директор Державного фармакологічного центру Міністерства охорони здоров’я Віктор Чумак. — Свого часу у Львові був ажіотаж, коли там випробовували препарати для лікування останньої, четвертої стадії онкозахворювання, результат був приголомшливий — у 30% випадків наступала ремісія.
Головна умова участі у випробуваннях — добровільна згода. В Україні законодавчо заборонено проводити дослідження на ув’язнених і військовослужбовцях.
Торік Верховна Рада прийняла поправки до Закону «Про лікарські препарати». Тепер випробування ліків на дітях строго контролюватимуться. Заборонено проводити дослідження ліків за участю дітей-сиріт.
— Загалом це найбільш скандальне і демагогічне питання. У нас діти забезпечені ліками всього на 40%, в інших випадках лікар радить мамі поділити дорослу таблетку і дати шматочок дитині. Ми потрапили в замкнуте коло: без клінічних досліджень саме на дітях не маємо права рекомендувати дитині лікарський препарат. Тому коли вони хворіють, ми їх труїмо дорослими ліками, ділячи таблетку на чотири частини, — говорить фармацевт.
Яким чином люди стають учасниками досліджень? Найчастіше — за рекомендацією свого лікаря, який бачить, що традиційні методи лікування неефективні. Іноді пацієнти знаходять інформацію про дослідження в Інтернеті і наполягають на своїй участі в проекті.
Ось лише один із прикладів. У жителя Запоріжжя Миколи Я. — проблеми з судинами. Операцію робити не можна через хворе серце. Коли лікар запропонував спробувати нові ліки, Микола погодився. Вживає їх уже два роки. Переваги є: безкоштовне лікування, постійний контроль лікарів, покращення стану здоров’я. Про ризик він намагається не думати. За законом, у разі ускладнень він має право на матеріальне відшкодування, проте ця перспектива досить примарна.
— Проблема страхування учасників клінічного дослідження в Україні залишається надзвичайно актуальною. Зазвичай суми страхових відшкодувань виявляються неналежними, а страхові угоди укладені таким чином, що отримати компенсацію за нанесену шкоду здоров’ю просто неможливо, — пояснює Василь Корнацький.
Відповідальність без покарання
— Звичайно, розмови про те, що ми полігон для експериментів, — це міф, — говорить президент Всеукраїнської ради захисту прав та безпеки пацієнтів Віктор Сердюк. — Навпаки, тут інша проблема. В Україні проводиться в шість разів менше клінічних досліджень, ніж могло бути. Одна з причин — замовники нам не довіряють, тому що в нас часто змінюються правила гри, а законодавча і нормативна бази не завжди відповідають міжнародним стандартам. Наприклад, таке питання: чи несуть медики відповідальність за погіршення здоров’я або смерть внаслідок прийому незареєстрованих ліків? Адже часто тяжкохворі сліпо довіряють лікарю і навіть не дивляться, що підписують. А згідно з українським законодавством, покарання лікаря за смерть пацієнта внаслідок клінічних досліджень передбачено лише в тому разі, якщо пацієнт не давав своєї згоди. Поза сумнівом, клінічні дослідження потрібні як країні, так і людям. Але для цього потрібно до чинної нормативної базі додати систему відповідальності та впровадити покарання за її невиконання.
Експерти вважають, що в умовах недостатнього бюджетного фінансування системи охорони здоров’я України в цілому та лікувально-профілактичних закладів зокрема проведення клінічних досліджень стане істотним внеском у фінансову стабільність значної кількості вітчизняних лікарень, проте сьогодні використовується лише 10–15% потенціалу України. Гострою проблемою залишається нормативно-правова неврегульованість обігу досліджуваних препаратів — їх ввезення, обліку, зберігання, знищення або повернення.
— Проблема, яка заважає збільшенню кількості досліджень, — розмитнення лікарських засобів, що надходять в Україну. Тобто це ще не ліки, це лише розробка. Але коли вони потрапляють на терени нашої держави, на них уже встановлюється величезний податок. Треба врегулювати це питання, враховуючи практику інших країн: якщо немає товару, відповідно, немає й ціни (дослідні препарати для пацієнтів безкоштовні), податок має бути мінімальним. Слід визначитися, в чому держава більш зацікавлена: отримати гроші зараз чи взяти участь у довгострокових перспективних дослідженнях, — зауважує Василь Корнацький.
ЦІКАВО ЗНАТИ
♦ До XX століття етичні питання медичної та дослідницької діяльності залежали лише від совісті лікарів, тож часто мали місце факти глобальних порушень етики з серйозними наслідками для здоров’я людей.
♦У III столітті до н. е. римські лікарі випробовували нові ліки тільки на засуджених до смертної кари злочинцях.
♦У XVI столітті, коли король Генріх II отримав поранення ока, придворні медики вибили очі чотирьом засудженим, щоб вивчити рану.
♦1769 року лікар Едуард Дженнер випробував на дітях сусідів першу вакцину, заразивши їх безпечною для людини свинячою віспою.
♦У 1805 році японський хірург Сейшен Ханаока вивчав на своїй дружині наслідки застосування наркозу (суміш із шести видів наркотиків і алкалоїдів).
♦У 1899 році в Прусії видається перший у світі закон, що забороняє лікарям ставити експерименти на людях без їхньої згоди.
♦У 1930 році в США досліджували природний перебіг сифілісу на 400 хворих, які не підозрювали про експеримент.
♦У 1937 році після випробування на пацієнтах сульфаніламіду — нового противірусного препарату — в США загинули 107 осіб.



 Ми в Google+
Ми в Google+